The capacidad calorífica específica o calor específico es la cantidad de calor que hay que aportar a la unidad de masa de una sustancia o sistema termodinámico para elevar su temperatura en una unidad. El calor específico depende del valor de la temperatura inicial. Se le representa con la letra c.
La capacidad calorífica es la cantidad de calor que hay que aportar a toda la masa de un material para elevar su temperatura en una unidad. Se la representa con la letra C.
La relación entre el calor específico y la capacidad específica, por tanto, es la masa del elemento. El calor específico es una propiedad que se puede definir para un elemento químico, mientras que para la capacidad calorífica es necesario conocer la masa.
Index
IMPORTANCIA CAPACIDAD CALORÍFICA
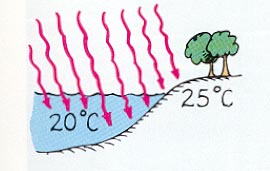
La capacidad calorífica tiene una gran importancia en muchos aspectos en los que nos movemos y en nuestro día a día. El primer aspecto sería el clima, a través del agua del océanos, que regulan el clima del planeta. Gracias a la alta capacidad calorífica del agua, se requiere mucho calor para subir su temperatura.
Esto hace que en zonas cercanas al mar, la temperatura durante el año sea más constante que en zonas alejadas. Al comienzo de verano la temperatura del agua es baja y aun haciendo mucho calor en la orilla, el agua no se calienta de forma inmediata, manteniendo un clima no tan caluroso. Al llegar al invierno el proceso es al revés, la temperatura del agua no baja tan rápido y mantiene un clima suave en el invierno.
CAPACIDAD CALORÍFICA DEL AGUA
En el caso particular del agua, el calor específico, c vale 1 cal/(g ºC) ó 4186 J(kg ºK). Esto quiere decir que se necesita 1 caloría para subir 1ºC la temperatura del agua. Se expresa en J/KgºK por que son las unidades de medida del Sistema Internacional, siendo en ese caso 4186 Julios para subir 1ºK 1Kg de agua.
Para obtener la capacidad calorífica de la masa hay que multiplicar el calor específico (en gramos o Kg, según las unidades que utilces) por la masa.
CALOR ESPECÍFICO DE ALGUNAS SUSTANCIAS
| Sustancia | Fase | cp |
| (másico) | ||
| J·g−1·K−1 | ||
| Gas monoatómico (Ideal) | gas | |
| Helio | gas | 5,1932 |
| Argón | gas | 0,5203 |
| Gas diatómico (Ideal) | gas | |
| Hydrogen | gas | 14,3 |
| Nitrógeno | gas | 1,04 |
| Oxygen | gas | 0,918 |
| Aire (en condiciones | gas | 1,012 |
| típicas de habitaciónnota 3) | ||
| Aluminio | sólido | 0,897 |
| Amoníaco | líquido | 4,7 |
| Antimonio | sólido | 0,207 |
| Arsénico | sólido | 0,328 |
| Berilio | sólido | 1,82 |
| Carbono (diamante) | sólido | 0,519 |
| Carbono (grafito) | sólido | 0,711 |
| Cobre | sólido | 0,385 |
| Diamante | sólido | 0,5091 |
| Ethanol | líquido | 2,44 |
| Gasolina | líquido | 2,22 |
| Oro | sólido | 0,1291 |
| Plata | sólido | 0,237 |
| Grafito | sólido | 0,71 |
| Hierro dulce | sólido | 0,45 |
| Níquel | sólido | 0,444 |
| Plomo | sólido | 0,129 |
| Wolframio | sólido | 0,133 |
| Titanio | sólido | 0,523 |
| Litio | sólido | 3,58 |
| Magnesio | sólido | 1,02 |
| Mercurio | líquido | 0,1395 |
| Neón | gas | 1,0301 |
| cera de parafina | sólido | 2,5 |
| Sílice (fundido) | sólido | 0,703 |
| Uranium | sólido | 0,116 |
| Water | gas (100 °C) | 2,08 |
| Water | líquido (25 °C) | 4,1813 |
| Water | sólido (0 °C) | 2,05 |
| Alúmina Al2O3 | sólido | 0,16 |
| MgO | sólido | 0,457 |
| SiC | sólido | 0,344 |
| Nylon 66 | sólido | 1,20-2,09 |
| Fenólicos | sólido | 1,40-1,67 |
| Polietileno (AD) | sólido | 1,92-2,30 |
| Polipropileno | sólido | 1,88 |
| Politetrafluoretileno | sólido | 1,05 |
| Todas las medidas son a 25 °C a menos que se indique lo contrario, | ||
